Toda formulação cosmética tem a indicação do pH ideal para aquele produto e ele é de extrema importância, pois se não estiver adequado pode causar sérias lesões e danos na pele e no couro cabeludo. Por isso é importante entender melhor o que é o pH. Confira!
COMO O pH É POSSÍVEL?
Para entender como o pH é possível, primeiramente temos que entender um pouco sobre os íons. O íon é um átomo ou molécula com carga elétrica, assim quando uma molécula se ioniza, divide-se em duas, criando um par de íons com cargas elétricas opostas, ou seja, um com carga elétrica negativa (ânion), e um com carga elétrica positiva (cátion).
Uma molécula de água, por exemplo, é composta por dois átomos de hidrogênio e um de oxigênio, mas algumas de suas moléculas não permanecem unidas. Por causa da ionização natural da água, algumas moléculas se ionizam (dividem) em dois íons separados: H+ e OH–.
de hidrogênio e um de oxigênio, mas algumas de suas moléculas não permanecem unidas. Por causa da ionização natural da água, algumas moléculas se ionizam (dividem) em dois íons separados: H+ e OH–.
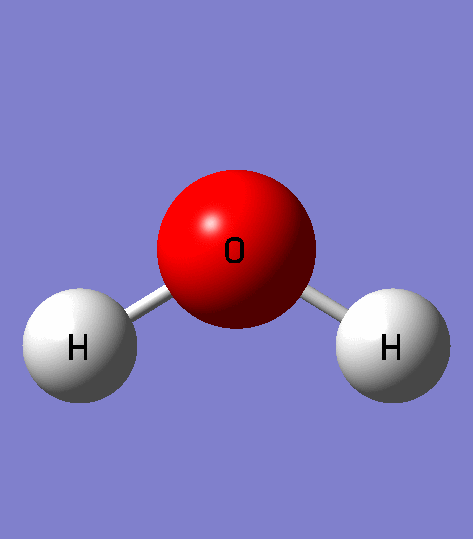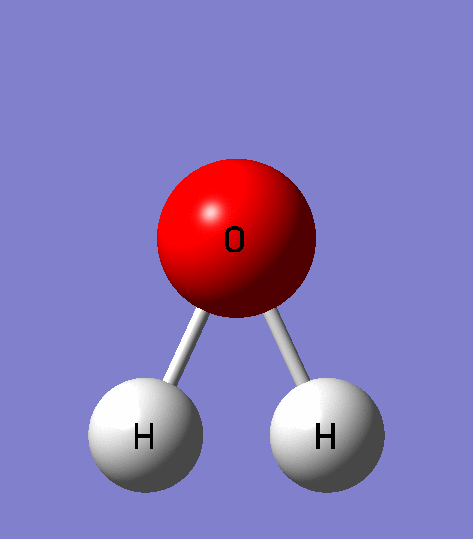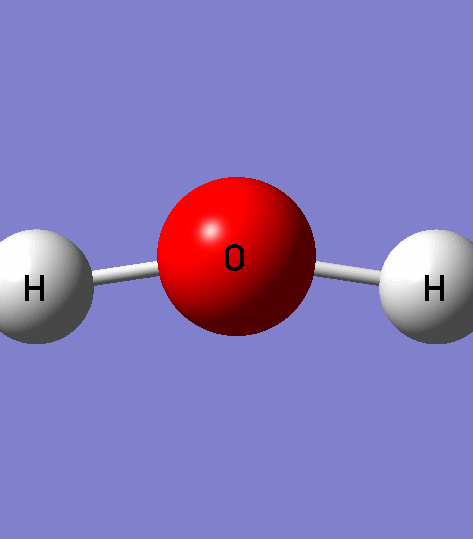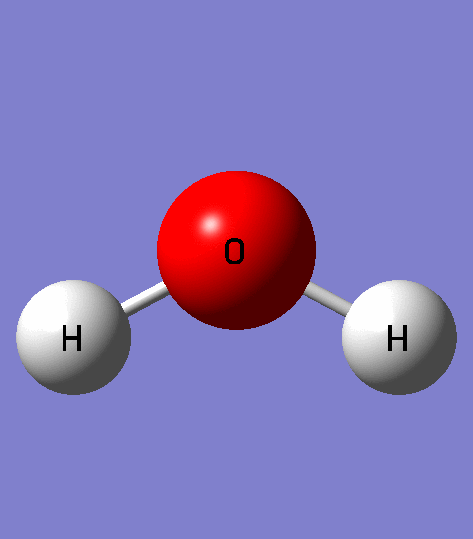 H+ é o íon de hidrogênio, ácido. OH– é o íon de hidróxido, alcalino. Toda molécula de água ao se ionizar rende um íon de hidrogênio (H+) e um de hidróxido (OH–). Dessa forma, por causa da ionização da água que o pH se torna possível, pois é possível se associar a outros íons.
H+ é o íon de hidrogênio, ácido. OH– é o íon de hidróxido, alcalino. Toda molécula de água ao se ionizar rende um íon de hidrogênio (H+) e um de hidróxido (OH–). Dessa forma, por causa da ionização da água que o pH se torna possível, pois é possível se associar a outros íons.
E é por isso também que somente substâncias aquosas têm pH, soluções não aquosas, como álcool e óleos, balms e bastões anidros, por exemplo, não possuem pH. Então para que exista o pH é essencial a presença de água.
Mas o que seria o pH?
ENTENDENDO O pH
pH significa potencial hidrogeniônico. O pH é uma medida físico-química para a concentração de íons hidrogênio em uma solução. Isso significa que o pH é relativo à quantidade de íons H+ e OH- liberados por uma determinada substância quando a mesma é dispersa em água.
Se a quantidade de íons H+ for maior do que a quantidade de íons OH-, dizemos que a substância é ácida. Por outro lado, se a quantidade de íons OH- for maior do que a quantidade de íons H+, dizemos que a substância é básica (ou alcalina).
E como sabemos o valor do pH?
Através de uma escala. As escalas são utilizadas para medir quantidades, como uma régua, que é usada para medir comprimentos. Da mesma forma é a escala de pH, ela mede os íons, indicando a acidez, neutralidade ou a alcalinidade por meio da medição da concentração de íons de hidrogênio em uma solução aquosa.
 A escala de pH tem origem no termo dinamarquês potenz hydrogen, ou potência de hidrogênio, proposta pela primeira vez em 1909 pelo químico dinamarquês Soren Peter Lauritz Sorensen para expressar concentrações dos íons hidrogênio no controle de qualidade de cervejas.
A escala de pH tem origem no termo dinamarquês potenz hydrogen, ou potência de hidrogênio, proposta pela primeira vez em 1909 pelo químico dinamarquês Soren Peter Lauritz Sorensen para expressar concentrações dos íons hidrogênio no controle de qualidade de cervejas.
A escala varia de 0 a 14, sendo que o valor 0 corresponde ao mais ácido, 7 ao neutro e 14 ao mais alcalino ou básico.
Então o número 7 divide a escala, assim um pH abaixo de 7 indica que é uma solução ácida e acima de 7 uma solução alcalina (básica).
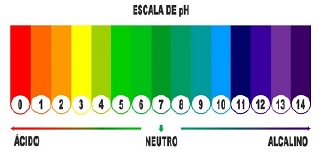
A alcalinidade aumenta quando o pH aumenta. Assim, um pH mais alto (com um número maior) é mais alcalino ou básico que um pH baixo (com número menor). Por exemplo, uma solução com pH 12 é mais alcalina do que uma solução com pH 9.
Em contrapartida, a acidez aumenta à medida que o pH diminui. Isso significa que um pH mais baixo(número menor) é mais ácido que um pH mais alto (número maior). Por exemplo, uma solução com pH 2 é mais ácida que uma solução com pH 5.
Já um pH 7 é considerado uma solução neutra, como é o casso da água pura. Uma molécula de água ao se ionizar rende um íon de hidrogênio (H+) e um de hidróxido (OH-). Por isso, em água pura, a concentração de ácidos e álcalis (bases) é igual, pois, cada vez que um íon de hidrogênio é produzido, um íon de hidróxido também é produzido.
Dessa forma, a água pura é neutra porque não é ácida nem alcalina. Ela é formada por um equilíbrio, ou seja, contém o mesmo número de íons de hidrogênio (H+) e de íons de hidróxido (OH-), sendo 50% ácida e50% álcali (básica).
Uma curiosidade interessante é que pH é escrito com p minúsculo. Você sabe por quê?
A princípio, a letra “p” foi utilizada significando Potenz (potência), na língua alemã, para descrever a magnitude da concentração de íons de hidrogênio, correspondendo à potência negativa de 10.
Esse fato sustentado por um de artigos de Sorensen cujas próprias palavras (traduzidas do alemão) diz:

“A magnitude da concentração de íons de hidrogênio será representada por meio do fator de normalidade em relação ao íon de hidrogênio, e esse fator será escrito na forma de um potenz negativo (potência) de 10. Uma vez que me refiro ao acima em uma seção posterior (ver página159), mencionarei aqui apenas que emprego o nome “expoente do íon hidrogênio” e o símbolo pH para o valor numérico deste potenz (potência). “
Mas até hoje a origem exata do p minúsculo no pH ainda é debatida. A princípio, alguns estudiosos afirmam que foi arbitrário, utilizando p e q para rotular a solução de ensaio e a solução de referência.
 Mas o fato é que o símbolo mudou ao longo dos anos, passando por uma variedade de símbolos, como “PH +”, “ph” e “Ph”. Até que em 1920, em uma publicação, o“P” foi escrito de forma minúscula aparentemente por conveniência tipográfica. E acabou tornando-se convenção devido à sua adoção pelo amplamente divulgado Journal of Biological Chemistry.
Mas o fato é que o símbolo mudou ao longo dos anos, passando por uma variedade de símbolos, como “PH +”, “ph” e “Ph”. Até que em 1920, em uma publicação, o“P” foi escrito de forma minúscula aparentemente por conveniência tipográfica. E acabou tornando-se convenção devido à sua adoção pelo amplamente divulgado Journal of Biological Chemistry.
Atualmente, este “p” minúsculo é aceito e formalmente utilizado para expressar, em química, uma constante de acidez. Acontece que, na Química, os cologaritmos (logaritmos do inverso de um número)decimais são representados por um ‘p’ minúsculo.
Já o H é o símbolo do elemento hidrogênio e é padrão colocar símbolos de elemento em maiúscula.
Outra curiosidade interessante é que conhecemos os valores de pH em uma escala colorida que vai do vermelho ao azul, por causa dos indicadores de pH que adquirem essas colorações de acordo com o pH das soluções em que são adicionados. Alguns dos indicadores de pH mais comuns usados em laboratório estão a fenolftaleína, o alaranjado de metila, o azul de bromotimol e o papel de tornassol.
Mas você sabe como o pH influencia a vida cotidiana?
 O pH tem um importante papel no estômago, na digestão dos alimentos. O ácido clorídrico (HCl), um componente do suco gástrico, é fundamental para criar o pH necessário para que a pepsina – a principal enzima envolvida na digestão de proteínas, assuma sua forma ativa e faça a digestão dos alimentos.
O pH tem um importante papel no estômago, na digestão dos alimentos. O ácido clorídrico (HCl), um componente do suco gástrico, é fundamental para criar o pH necessário para que a pepsina – a principal enzima envolvida na digestão de proteínas, assuma sua forma ativa e faça a digestão dos alimentos.
O pH também desempenha um importante papel no solo, no crescimento de plantas e culturas, uma vez que o pH ideal para um bom crescimento das plantas está entre 6,3 e 7,3.
Até para prevenir cárie dentária o pH é importante. Certos alimentos aumentam a acidez da boca, diminuindo assim o nível de pH. A saliva ajuda a neutralizar o excesso de ácido, mas isso pode levar de alguns minutos a algumas horas para que o pH da boca seja neutralizado, e durante esse tempo, o baixo pH da boca cria um ambiente ideal para bactérias ruins, que eventualmente causam cáries.
 E em produtos cosméticos o pH também é de extrema importância, porque o nosso pH natural sofre alterações conforme a região do corpo, idade, e dependendo da finalidade, se o pH do produto for diferente do natural, pode causar sérias lesões e danos na pele e no couro cabeludo.
E em produtos cosméticos o pH também é de extrema importância, porque o nosso pH natural sofre alterações conforme a região do corpo, idade, e dependendo da finalidade, se o pH do produto for diferente do natural, pode causar sérias lesões e danos na pele e no couro cabeludo.

Veja também “ESCOVA PROGRESSIVA: TUDO SOBRE O ÁCIDO GLIOXÍLICO”.
Deixe seu comentário, dicas e sugestões. Pesquise em nosso Blog e compartilhe com os amigos. Curta nossa página no Facebook e vejas novidades no nosso canal do YouTube.
Referências
Heda, R., Toro, F. e Tombazzi, CR (atualizado em 2020, 24 de maio). Fisiologia, pepsina. StatPearls.Disponível em: https://www.ncbi.nlm.nih.gov/books/NBK537005/
Gentili, R., Ambrosini, R., Montagnani, C., Caronni, S. e Citterio, S. (2018, 20 de setembro). Efeito do pHdo solo no crescimento, investimento reprodutivo e alergenicidade ao pólen de Ambrosia artemisiifolia L.Front Plant Sci. Disponível em: https://www.frontiersin.org/articles/10.3389/fpls.2018.01335/full
Dawes, C. (2003, dez). Qual é o pH crítico e por que um dente se dissolve em ácido? Disponível em:https://pubmed.ncbi.nlm.nih.gov/14653937/
Cosmetics and Toiletries. Vol. 136, No. 5, May 2021. Formulating Forum pH Precision- HarmonizingCosmetics with the Microbiome. Disponível em: https://www.cosmeticsandtoiletries.com/formulas-products/skin-care/article/21836092/cosmetics-toiletries-magazine-formulating-forum-ph-precision







Comments
Eu observei no texto o que eu acredito ser OH com sinal de menos…
Procede? Estou pesquisando bastante para entender de pH.
Desde já obrigada.
Author
Olá Rose!
É isso mesmo.
Obrigada por nos avisar do erro de digitação.
Abraços!